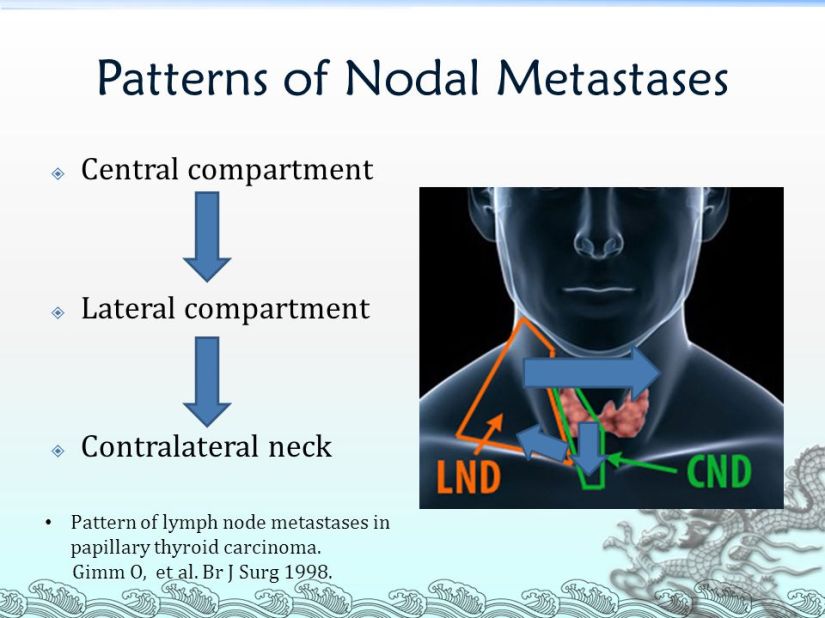
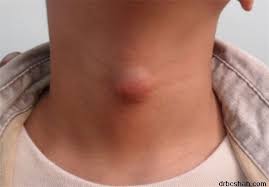
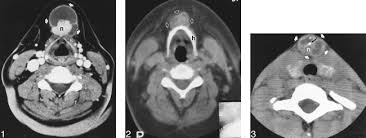
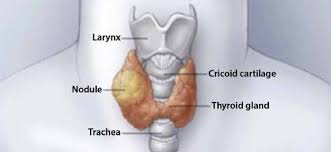
31 yo male with a history of testicular seminoma (January 2018) that underwent a PET/CT for follow up and identified a focal area of increase uptake (SUV 10) on the right thyroid lobe.
Ultrasound confirmed that the focal area increase uptake correlated to a thryoid nodule (ultrasonographic pattern with intermediate suspicion of malignancy). FNAB reveal a papillary thyroid carcinoma (PTC) (Bethesda IV).
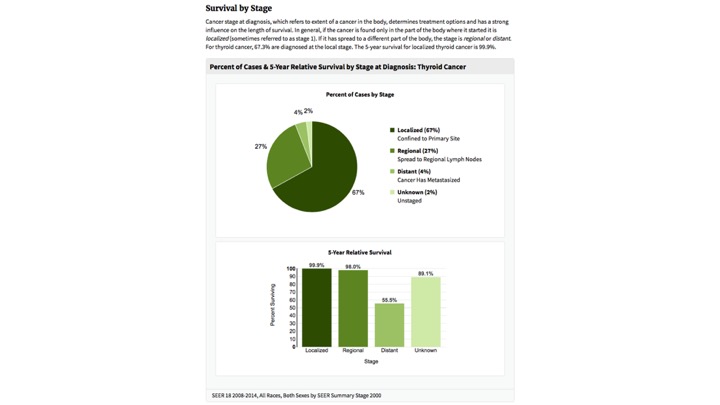
Clinical staging: cT2, cN0, cM0 (Stage 1)
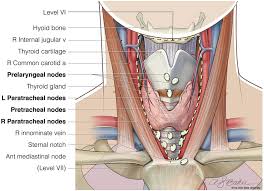
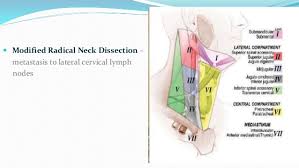
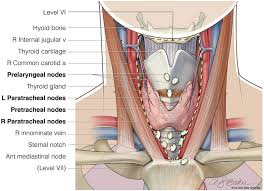
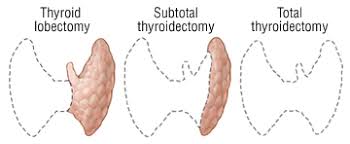
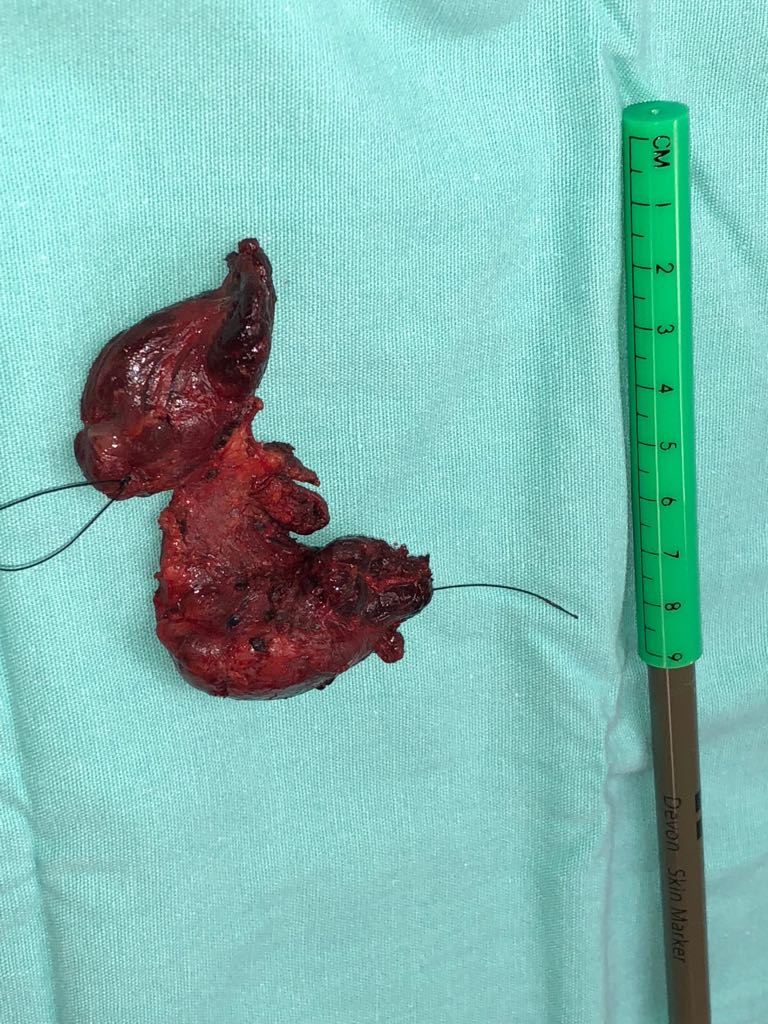
A total thyroidectomy with ipsilateral prophylatic central compartment neck dissection.
Pathologic staging: pT2(s), pN1a, cM0 (stage I)
Tumor Size 2.3 cm X 1.7 cm
PTC Hobnail variant (15% of cells had the Hobnail characteristics)
No extrathryoidal extension
Vascular invasion (4 foci)
No perineural invasion
Margens negative
Ipsilateral central compartment dissection
Total 9 lymph nodes were harvested
5 lymph nodes positive for PTC (largest metastatic foci 3 mm)
MACIS (7 high risk) – 3.73
AGES (≤4 low risk; >4 high risk) – 3.42
AMES – Low risk
ATA classification – Intermediate risk of recurrence (risk of recurrance above 20%)
Case performed by a member of Sociedad Quirúrgica S.C.:
Rodrigo Arrangoiz MS, MD, FACS expert in the management of thyroid diseases.
Training:
• General surgery:
• Michigan State University:
• 2004 al 2010

• Surgical Oncology / Head and Neck Surgery / Endocrine Surgery:
• Fox Chase Cancer Center (Filadelfia):
• 2010 al 2012

• Masters in Science (Clinical research for health professionals):
• Drexel University (Filadelfia):
• 2010 al 2012

• Surgical Oncology / Head and Neck Surgery / Endocrine Surgery:
• IFHNOS / Memorial Sloan Kettering Cancer Center:
• 2014 al 2016