Mujer 32 años con carcinoma papilar de tiroides cT2, cN0, cM0 estadio I
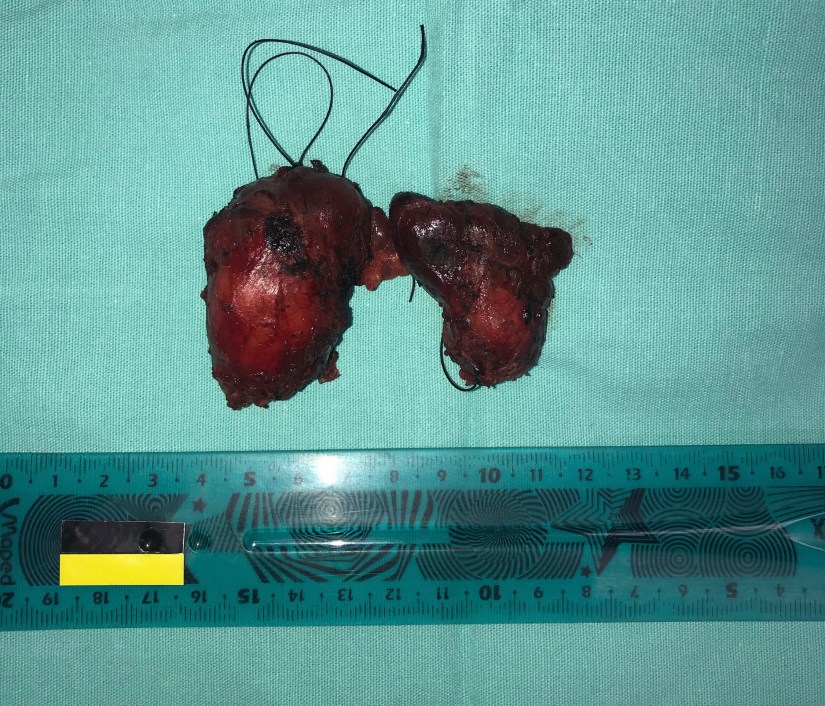
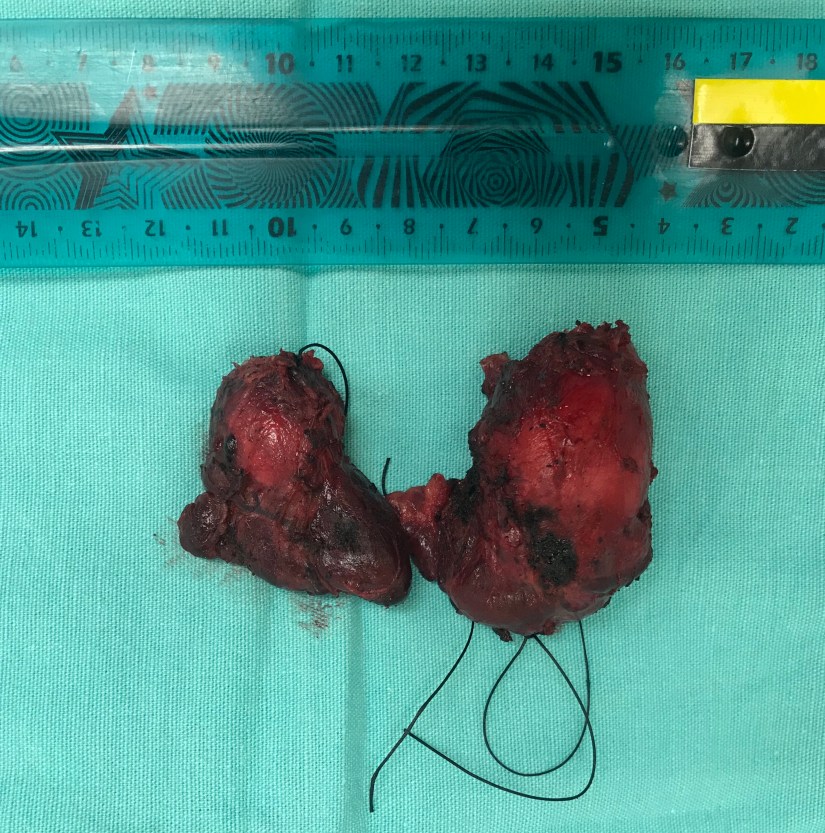
Mujer 32 años con carcinoma papilar de tiroides cT2, cN0, cM0 estadio I


http://www.cirugiatiroides.com
Rodrigo Arrangoiz MS, MD, FACS cirujano de tumores de cabeza y cuello / cirugia endocrina / cirugía oncológica es experto en el manejo de patología de la glándula tiroides.
Su entrenamiento fue el siguiente:
• Cirugia general y gastrointestinal:
• Michigan State University:
• 2004 al 2010
Cirugia oncológica / tumores de cabeza y cuello / cirugia endocrina:
• Fox Chase Cancer Center (Filadelfia):
• 2010 al 2012
• Maestria en ciencias (Clinical research for healthprofessionals):
• Drexel University (Filadelfia):
• 2010 al 2012
• Cirugia de tumores de cabeza y cuello / cirugiaendocrina
• IFHNOS / Memorial Sloan Kettering Cancer Center:
• 2014 al 2016








 • Cirugia oncológica / tumores de cabeza y cuello / cirugia endocrina:
• Cirugia oncológica / tumores de cabeza y cuello / cirugia endocrina: • Maestria en ciencias (Clinical research for healthprofessionals):
• Maestria en ciencias (Clinical research for healthprofessionals): • Cirugia de tumores de cabeza y cuello / cirugiaendocrina
• Cirugia de tumores de cabeza y cuello / cirugiaendocrina
Click to access IJOHNS_2017072615211601.pdf
Click to access IJOHNS_2018071317420392.pdf
 • Cirugia oncológica / tumores de cabeza y cuello / cirugia endocrina:
• Cirugia oncológica / tumores de cabeza y cuello / cirugia endocrina: • Maestria en ciencias (Clinical research for healthprofessionals):
• Maestria en ciencias (Clinical research for healthprofessionals): • Cirugia de tumores de cabeza y cuello / cirugiaendocrina
• Cirugia de tumores de cabeza y cuello / cirugiaendocrina
 • Cirugia oncológica / tumores de cabeza y cuello / cirugia endocrina:
• Cirugia oncológica / tumores de cabeza y cuello / cirugia endocrina: • Maestria en ciencias (Clinical research for healthprofessionals):
• Maestria en ciencias (Clinical research for healthprofessionals): • Cirugia de tumores de cabeza y cuello / cirugiaendocrina
• Cirugia de tumores de cabeza y cuello / cirugiaendocrina
El hiperparatiroidismo primario esporádico se debe a:
http://www.sociedadquirurgica.com
http://www.hiperparatiroidismo.info
 • Cirugia oncológica / tumores de cabeza y cuello / cirugia endocrina:
• Cirugia oncológica / tumores de cabeza y cuello / cirugia endocrina: • Maestria en ciencias (Clinical research for healthprofessionals):
• Maestria en ciencias (Clinical research for healthprofessionals): • Cirugia de tumores de cabeza y cuello / cirugiaendocrina
• Cirugia de tumores de cabeza y cuello / cirugiaendocrina